生命科学学院王敬文研究员课题组 在按蚊传播疟原虫机制方面取得新发现
近日,复旦大学生命科学学院王敬文研究员课题组通过解析按蚊免疫系统-肠道菌群-围食膜-疟原虫四者之间的相互作用,揭示了疟疾传播媒介按蚊免疫系统调控肠道菌群抵抗疟原虫感染的新机制。2月28日,相关研究成果以《斯氏按蚊肽聚糖识别蛋白PGRP-LD通过调控肠道菌群诱导的围食膜形成影响按蚊的载体效能》(PGRP-LD mediates A. stephensi vector competency by regulating homeostasis of microbiota-induced peritrophic matrix synthesis)为题在线发表于《病原体》( Plos Pathogens )。
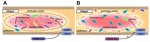
研究发现,疟疾传播媒介斯氏按蚊的免疫识别受体PGRP-LD通过负调控免疫系统,保护体内肠道菌群,而健康的肠道菌群促进完整围食膜的形成,有效阻碍疟原虫感染。图为PGRP-LD作用模式图。
肽聚糖识别受体家族(PGRP)是昆虫中重要的一类免疫识别受体,具有启动免疫信号通路和调控免疫反应强度的作用。PGRP-LD在果蝇和多种虫媒中广泛存在,但至今为止,其功能尚不清楚。课题组利用RNA干扰的方法敲低PGRP-LD后发现,与对照相比,免疫反应的效应分子表达水平显著上升,但是按蚊对疟原虫更加易感,说明免疫反应激活不能有效清除疟原虫。同时,免疫反应的激活破坏了按蚊体内肠道菌群的稳态,导致菌群数量显著下调,且肠内空间分布发生变化。
课题组进一步研究发现,敲低PGRP-LD后,菌群空间分布的变化是由于围食膜破损导致的。围食膜是昆虫体内由几丁质、糖蛋白等组成的一类非细胞的鞘状结构,主要负责包裹昆虫所摄入的食物及其有害物质,保护机体免受摄入物质的损伤。该研究发现,按蚊体内围食膜的形成受肠道菌群调控,当菌群数量下降或者缺失时,围食膜相关基因表达水平发生变化,导致围食膜结构受损或者无法形成。当在按蚊中回殖入一定数量的肠道菌后,围食膜形成恢复,且对疟原虫易感性降低。以上结果说明,按蚊免疫系统通过保护肠道菌群促进完整围食膜的形成,从而有效阻碍疟原虫在按蚊体内的发育。
复旦大学生命科学学院硕士研究生宋秀梅为本文的第一作者,复旦大学生命科学学院王敬文研究员为本文的通讯作者。该研究获得国家自然科学基金委、国家重点研发计划及美国NIH RO1项目的支持。