生物医学研究院周玉峰课题组揭示甘露糖受体调节过敏性炎症反应的新机制
近日,生物医学研究院周玉峰课题组和约翰霍普金斯大学医学院Peisong Gao教授合作揭示了甘露糖受体调节过敏性炎症反应的新机制--通过miR-511-3p调节巨噬细胞极化。相关研究成果以《甘露糖受体通过miR-511-3p调节巨噬细胞极化和过敏性炎症》 (Mannose Receptor Modulates Macrophage Polarization and Allergic Inflammation through miR-511-3p)为题在线发表于《变态反应与临床免疫学杂志》(Journal of Allergy and Clinical Immunology,JACI)杂志。周玉峰研究员为第一作者。
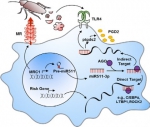
甘露糖受体(Mannose receptor,MR)属于C型凝集素超家族成员,可通过胞外区识别和结合特定的糖类分子,在识别病原体、递呈抗原和保持内环境稳定中发挥作用。该研究发现甘露糖受体基因敲除可以影响巨噬细胞极化,表现为M1巨噬细胞极化增强,而M2巨噬细胞极化减弱,MR基因敲除鼠体内过敏反应增强。但甘露糖受体细胞内部分非常短,缺乏细胞内信号转导结构,一个缺乏信号转导功能的受体分子如何影响细胞极化,这非常难于解释。研究者对MR基因分析后发现,MR基因第五内含子含有microRNAs(miR-511-3p), 甘露糖受体与miR-511-3p协同表达,miR-511-3p可抑制M1极化, MR通过协同表达的miR-511-3p调节巨噬细胞极化而调节过敏性炎症。
研究发现miR-511-3p在体内外均有抗炎作用,可用于哮喘治疗。同时发现过敏性哮喘病人体内miR-511-3p明显降低,可用于哮喘诊断。该研究为哮喘,特别是难治性哮喘的诊断和治疗提供了新策略和方法。该项研究受到中国国家自然科学基金和美国NIH基金的资助。