鲁伯埙课题组揭示激酶介导的神经退行性亨廷顿病 致病蛋白水平的正反馈调控机制
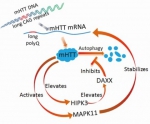
蛋白激酶MAPK11和HIPK13正反馈调控变异HTT水平的模式图
近日,复旦大学鲁伯埙课题组针对神经退行性病变亨廷顿病的研究取得重要突破,发现了变异HTT蛋白积累的正反馈机制,对亨廷顿病 (Huntington’s Disease,HD)疾病机制的理解提供了全新视角。此外,研究揭示了mHTT蛋白调控的激酶基因MAPK11及HIPK3,为HD疾病治疗提供了潜在新药靶。相关研究成果以《抑制MAPK11或HIPK3降低亨廷顿舞蹈病模型中的突变型亨廷顿蛋白水平》(Suppression of MAPK11 or HIPK3 Reduces Mutant Huntingtin Levels in Huntington’s Disease Models)为题发表在《细胞研究》(Cell Research)上。该研究为神经退行性病变亨廷顿病的药物研发提供两个重要靶点,并可能推广至类似疾病。
神经退行性疾病引起中枢神经系统特定神经元不正常死亡萎缩,导致神经功能严重缺陷,认知或运动功能障碍,是最重要的神经疾病之一。目前此类疾病尚没有可以改变疾病进程的根本性治疗方法。是神经退行性疾病中最主要的单基因遗传病。由于其遗传图景清晰,是此类疾病重要的模式疾病。遗传学证据表明,HD主要由突变基因HTT所表达的突变HTT蛋白的神经毒性所导致,因此HTT蛋白如何调控以及如何降低HTT蛋白水平至关重要,并且可能为疾病治疗提供重要药靶。
鲁伯埙实验室在两株独立的亨廷顿病人成纤维细胞中,通过高通量遗传学筛选检测了2600多个潜在的药靶基因对HTT蛋白水平的影响,并进行了针对细胞存活的对照筛选,发现了19个HTT蛋白水平的潜在调控基因。鲁伯埙课题组进一步在人类干细胞分化的亨廷顿病神经元进行了进一步筛选,检测变异HTT水平与神经元的存活,发现两者存在明显的负相关,系统性地证明了通过调控基因降低HTT蛋白水平可以增加神经元存活。其中,敲减11个HTT的调控基因在此神经元模型中也可以显著降低变异HTT水平并增加神经元存活。课题组选定这11个与HTT调控相关的基因进行深入研究。
鲁伯埙课题组验证了这11个基因中的两个激酶基因,MAPK11和HIPK3。两者在病人脑部神经元均有明显表达。敲减MAPK11或者HIPK3均能在各种亨廷顿病细胞模型(即HTT突变型细胞,HD细胞)及动物模型中显著降低HTT水平。有趣的是,这两个激酶只在HD细胞中才对HTT蛋白有调控作用,而在野生型细胞中没有发现这个现象。进一步实验证实MAPK11和HIPK3对HTT蛋白的调控依赖于变异HTT蛋白的存在,这是因为变异HTT蛋白会激活MAPK11和HIPK3,这样形成了正反馈循环,加速了疾病蛋白的积累,并由此参与了疾病的发生发展。研究进一步发现激酶MAPK11和HIPK3调控变异HTT蛋白水平的机制。 MAPK11通过调控HTT mRNA的稳定性调控HTT蛋白水平,而HIPK3则通过磷酸化其底物DAXX调控自噬水平而影响HTT蛋白的降解。鲁伯埙课题组进一步检测了MAPK11和HIPK3作为亨廷顿病药靶的潜在可能性。MAPK11及HIPK3对HTT的调控均依赖于其各自激酶活性,而MAPK11和HIPK3的抑制剂在亨廷顿神经细胞模型中均能显著降低HTT蛋白水平,为靶向MAPK11或HIPK3的亨廷顿病的药物研发提供了分子水平实验验证。
本研究还在基因敲入的亨廷顿病小鼠在体模型中对MAPK11及HIPK3进行了验证。敲除MAPK11或HIPK3均能显著降低HTT蛋白水平与聚集,但敲除MAPK11起作用相对较早。小鼠行为学实验则证明敲除MAPK11可以有效挽救/缓解亨廷顿病小鼠的疾病引起的运动能力障碍,为靶向MAPK11提供了在体证据。
鲁伯埙研究员多年来潜心致力于亨廷顿疾病发生发展机制研究,已在Nature Neuroscience、Nature Chemical Biology、eLife等著名期刊上发表论文多篇。
博士生于梦、博士后付玉华及博士生梁益坚为论文第一作者,复旦大学是文章的第一单位及唯一通讯单位,鲁伯埙研究员为本论文唯一通讯作者。该项研究获得国家自然科学基金重大研究计划培育项目及优青项目支持。